Oxizi de azot
Oxizii de azot sunt combinații chimice sub formă gazoasă ale azotului în raporturi diferite cu oxigenul în funcție de gradul de oxidare. Oxizii de azot sunt combinații chimice care nu iau naștere spontan ci numai prin absorbție de energie, cu excepția protoxidului de azot care este folosit ca narcotic. Ceilalți oxizi formează în contact cu apa acizi, liberi în aer sub acțiunea razelor UV eliberează ozon fiind dăunător mediului înconjurător.
| Legătura azotului | formula chimică | Denumire |
| +1 | N2O |
protoxid de azot |
| +2 | NO |
monoxid de azot |
| +3 | N2O3 |
trioxid de azot |
| +4 | NO2 |
dioxid de azot |
| +4 | N2O4 |
tetraoxid de azot |
| +5 | N2O5 |
pentaoxid de azot |
Gaze nitrice
Gaze nitrice sunt denumite oxidul (NO) și bioxidul de azot (NO2). Ele iau naștere prin reacția acidului azotic (HNO3) cu metale, substanțe organice, sau prin arderea cărbunilor și produselor petroliere.
Acțiunilor oxizilor de azot
- produc iritarea, lezarea căilor respiratorii
- favorizează formarea ploilor acide
- (2NO2 + H2O → HNO3 + HNO2)
- favorizează formarea smogului
- favorizează formarea ozonului sub acțiunea razelor ultra violete
 Monoxid de azot, NO
Monoxid de azot, NO Dioxid de azot, NO2
Dioxid de azot, NO2 Protoxid de azot, N2O
Protoxid de azot, N2O Trioxid de diazot, N2O3
Trioxid de diazot, N2O3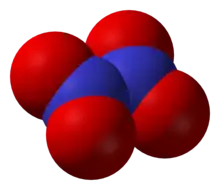 Tetroxid de diazot, N2O4
Tetroxid de diazot, N2O4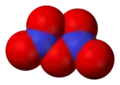 Pentoxid de diazot, N2O5
Pentoxid de diazot, N2O5
Bibliografie
- Linus Pauling, Chimie generală, Editura Științifică, București, 1972 (traducere din limba engleză)
- Raluca Ripan, I. Ceteanu, Manual de lucrări practice de chimie anorganică - vol I Metaloizi, Editura de stat didactică și pedagogică, București, 1961
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.