Oxid de magneziu
Oxidul de magneziu este un compus binar al magneziului cu valență II cu oxigenul.
| Oxid de magneziu | |
 | |
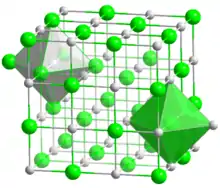 | |
| Nume IUPAC | Oxid de magneziu |
|---|---|
| Alte denumiri | Magnezie |
| Identificare | |
| Număr CAS | 1309-48-4 |
| ChEMBL | CHEMBL1200572 |
| PubChem CID | 14792 |
| Informații generale | |
| Formulă chimică | MgO |
| Aspect | pudră albă |
| Masă molară | 40,3044 g/mol |
| Proprietăți | |
| Densitate | 3,58 g/cm3 |
| Starea de agregare | solidă |
| Punct de topire | 2 852 °C |
| Punct de fierbere | 3 600 °C |
| Presiune de vapori | 0 millimetre of mercury[1] |
| Fraze R | R36, R37, R38 |
| NFPA 704 | |
0
1
0
| |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Obținere
Se poate obține foarte simplu, în laborator, prin arderea magneziului în flacără. Reacția ce are loc este foarte luminoasă, în timpul oxidării magneziului putându-se observa apariția unei flăcări orbitoare.
Dacă oxidul de magneziu obținut este lăsat într-un recipient cu apă în care s-a lăsat soluție de fenolftaleină, se poate observa colorarea în roșu carmin datorată formării de hidroxid de magneziu:
- MgO + H2O = Mg(OH)2
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
